Nos acercamos al azúcar invertido… Desde siempre he sentido la necesidad, en mayor o menos grado, y más o menos obsesiva según casos particulares, de entender el porqué de las cosas. Esto me ha llevado a ser muy cansino en mi niñez (por limitarlo en el tiempo), a declinarme por las ciencias frente a las humanidades (a pesar de entusiasmarme igualmente),… y… ¿por qué? debe ser la pregunta que más he hecho en mi vida, la que me sigo haciendo con cualquier cosa que me interesa, que quiero saber cómo funciona, por qué sucede…
Últimamente estoy haciendo bastante helado. Una de las cosas que quería empezar a utilizar para obtener helados más cremosos es el azúcar invertido… ¿pero qué es?, ¿por qué se llama así?, ¿cuál es el límite al que se puede llevar? Empecé a investigar y a repasar mis escasos conocimientos de química hasta (creer) llegar a entenderlo, que todo me cuadrara y hacer un par de experimentos… De ahí el nombre de la entrada, comprendiendo, desgranando, aproximándonos… Me gustaban y parecían más acertadas un par de palabras anglosajonas, que hubieran podido sonar pretenciosas, además de fuera de lugar, y no tuve cuajo para un el azúcar invertido y su p*** madre 😉 . Bueno ahí va el repaso de química.
¿Qué es el azúcar? El térmico azúcares se emplea para referirse a los monosacáridos, disacárido y polisacárido; es frecuente que se malutilice para referirse a cualquier glúcido o carbohidratos, del que son una parte. Por azúcar, sin más, azúcar común, la que compramos, la que echamos al café y los postres, nos referimos a la sacarosa.
La sacarosa es un disacárido (como la lactosa, maltosa, isomaltosa, trehalosa), es decir, es una molécula estable compuesta por dos monosacáridos: glucosa y fructosa en concreto. Su fórmula química no desarrollada es C12H22O11. Para ser más exactos: beta-D-fructofuranosil-(2->1)-alfa-D-glucopiranósido.
Esto quiere decir:
α y β (alfa y beta) hacen referencia al anómero, posición del grupo hidroxilo (alcohol, OH) en la molécula ciclada.
D y L hacen referencia al isómero óptico o enantiómero, por resumir, hacia dónde desvían la luz polarizada. D, dextrógiro (+) hacia la derecha y L, levógiro (-) hacia la izquierda. El 2 y el 1 hacen referencia a los carbonos que intervienen en la reacción.
Se presenta en estado sólido, en forma de cristales blancos (que todos conocemos), su densidad es 1587 kg/m3, su masa molas es de 342,3 g/mol, funde a 186ºC y su solbilidad en agua es de 204g/100ml (a 20ºC). La sacarosa es D-sacarosa, es decir, dextrógira
¿Qué es el azúcar invertido? Es un jarabe o solución de fructosa y glucosa; los monosacáridos que componen el azúcar. El término invertido hace referencia al comportamiento frente a la luz polarizada. La sacarosa, punto de partida, es dextrógira (+66,5º) al igual que la glucosa (+52,5º), mientras que la fructosa es levógira (-92º). Por tanto las propiedades ópticas quedan invertidas de dextrógiras en la sacarosa a levógiras en el azúcar invertido; de ahí su nombre.
¿Por qué el azúcar invertido? El azúcar invertido es, básicamente, una solución de fructosa y glucosa. Se da de forma natural en productos como la miel, al elaborar confituras,… y los seres vivos «invierten» la sacarosa antes de absorber o procesar la fructosa o lactosa; azúcares más sencillos y más fácilmente transformables y asimilables por los seres vivos.
Las aplicaciones culinarias más interesantes son:
- Mayor poder endulzante. La fructosa es mucho más dulce que la sacarosa, hasta 170% especialmente percibida en frío (muy útil para bebidas y refrescos); la glucosa lo es menos, un 70%. En general se habla de un 30% más de dulzor; no obstante Harold McGee habla de un 90%, entiendo que a temperaturas más elevadas.
- Mantiene más humedad en las masas.
- Acelera el ritmo de fermentación ya que los azúcares más sencillos son más fácilmente digestibles.
- Cristaliza a una temperatura mucho menor. Útil para la elaboración de helados.
¿Cómo se obtiene? El azúcar o sacarosa se invierte por hidrólisis: en presencia de agua, que actúa activamente en el proceso. La hidrólisis puede ser enzimática, como ocurre en los seres vivos, o ácida a alta temperatura, donde el ácido actúa como catalizador, dando pié pero no interviniendo directamente en la reacción.
A partir de un jarabe de sacarosa acidificado y aumentando la temperatura podemos romper el enlace que mantiene unidas la fructosa y glucosa en sacarosa y obtener estos monosacáridos por separado.
El ácido no interviene, sólo favorece o cataliza la reacción.
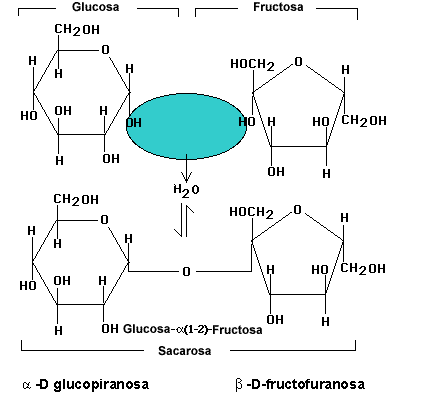
La reacción química que se da es la siguiente(en la imagen que hay arriba la reacción se lee de abajo a arriba con sumiéndose una molécula de agua): un mol de sacarosa reacciona con otro de agua dando como resultado un mol de sacarosa y otro de fructosa. Esto es:
C12H22O11 + H2O = C6H12O6 + C6H12O6
Una vez se consigue invertir la sacarosa, se puede neutralizar el ácido con una base: típicamente bicarbonato. En nuestro caso lo hicimos con ácido cítrico y bicarbonato sódico (papeletas de gaseosas). La reacción que se da al juntarlos libera CO2, por lo que se usa para gasificar agua o como impulsor repostero. Se puede utilizar otros ácidos como el tartárico (cremor tártaro); las papeletas contienen las cantidades justas para que la reacción de neutralización sea completa. En el caso del ácido cítrico la reacción es la siguiente: un mol de ácido cítrico reacción con tres moles de bicarbonato sódico dando lugar a un mol de citrato trisódico, tres de dióxido de carbono y 3 de agua. Esto es:
H3C6H5O7 + 3 NaHCO3 = Na3C6H5O7 + 3 CO2 + 3 H2O
Teniendo en cuenta las masas molares y la reacción ajustada por cada gramo de ácido cítrico necesitaremos 1,3 gramos de bicarbonato sódico. Cuadra con el contenido de las papeletas 😉
Ahora bien, una vez llegados a este punto, comprendido el proceso, dejamos un poco la teoría y vamos a la práctica y a preguntarnos qué queremos conseguir…
Las premisas de partida son las siguientes: quiero el azúcar invertido más concentrado posible en forma de jarabe para usar en helados. Quiero poder usar azúcar invertido añadiendo la menor cantidad posible de agua, como parte del jarabe, al helado. No quiero que cristalicen o precipiten azúcares en mi jarabe de azúcar invertido.
Por otro lado, en la mayoría de recetas que he encontrado por ahí hay dos coincidencias: la cantidad de azúcar es de unos 233 gramos por 100 gramos de agua y se recomienda reemplazar el 30% del azúcar original de la receta por azúcar invertido.
Si tenemos en cuenta las solubilidades de glucosa y fructosa vemos que son 91g/100ml y 375g/100ml respectivamente a 20ºC. Si hacemos el cálculo para cada monosacárido por separado, la cantidad de sacarosa para obtener una solución saturada de glocusa o fructosa, obviando el efecto del otro en la disolución en su solubilidad (que tenderá a disminuirla al estar más saturada la disolución) y teniendo en cuenta que por cada 342 gr de sacarosa podemos obtener 180 de glucosa y otro tanto de fructosa, tenemos:
Solución glucosa saturada: 170g sacarosa por cada 100g de agua aprox. (no estamos teniendo en cuenta el agua que se consume en la inversión).
Solución fructosa saturada: 700g sacarosa por cada 100g de agua aprox.(no estamos teniendo en cuenta el agua que se consume en la inversión).
Con estos números que obtuvimos (que además entendimos eran conservadores) las proporciones de la receta más común implicarían precipitación o cristalización de glucosa. Algo se me escapa… Así que me propuse hacer uno experimentos, tres pruebas con cantidades distintas de glucosa: 200g, 300g y 400g de sacarosa por 100g de agua. Además usé gaseosas de ácido cítrico(1,6g)/bicarbonato sódico(2,14g); en el caso de los 400g de azúcar usé dos: ahora creo que fue una estupidez, no hubiera habido ninguna diferencia.
El proceso es sencillo: disolver al calor el azúcar con el agua con la ayuda de una varilla. Evitar que sobrepase de los 80-90 grados para evitar evaporación, caramelización etc. Añadir el ácido (entiendo que esto puede hacerse de partida, no habría diferencia alguna) y distribuir bien. Mantener unos minutos caliente, al fuego a unos 80ºC para completar la inversión. Enfriar y neutralizar con el bicarbonato (entiendo que a cualquier temperatura funcionaría).
El resultado:
200g de sacarosa por 100g de agua: jarabe fluido a 5ºC.
300g de sacarosa por 100g de agua: se observan cristales a 5ºC. Se puede trabajar con el a pesar de ello.
400g de sacarosa por 100g de agua: muy denso y espumoso (quizá porque tenga mucho CO2 atrapado) no se observan cristales a 5ºC.
Conclusiones:
- Entre 200 y 300g parece el rango sensato donde moverse.
- Algo se me está escapando con el tema de la cristalización o precipitación. Puede que la velocidad de enfriamiento tenga influencia.
- No encuentro explicación para que no haya cristales con 400g y si con 300g, salvo que estos estuvieran ocultos por la estructura espumosa.
- No veo explicación a limitar al 30% el uso en helados; en repostería entiendo límites para controlar velocidades de fermentación y humedad residual.
- Experimentar es divertido.
- Como fastidia no ver llegar a entenderlo por completo.
Aquí os dejo un video donde podéis ver el aspecto de los resultados.








Espectacular Pablo. Me han dado ganas de volver a primero de carrera a estudiar orgánica. Gracias por este pedazo de post 🙂
Jejeje, muchas gracias! Es realmente reconfortante… Ayer a eso de las dos escribiendo sobre azúcares, para no llegar a mucha conclusión… Digamos que me sentí un poco freak cuanto menos.
La verdad es que me gusta bastante este tipo de ejercicios, rememorar tiempos de estudiante y esas cosas; ya sabes. Me he divertido bastante revisitando la orgánica (nunca supe nada…), intentando buscarle un poco de lógica, haciendo los experimentos… La verdad es que no tengo nada de base y hay bastantes cosas que se me escapan. Voy a ver si me documento un poco más y si lío a algún químico de confianza… Un beso.
afreirpimientos tv… jajajajajaja!
Llegas a cotas inimaginables de frikismo! Me han entrado ganas de probar alguno de esos fresisuis extradulces por pura curiosidad… Igual es lo que le falta a vuestros helados. Dentro de poco podrás hacer esos vídeos pero con Lucía en una esquina de la pantalla chupándose la mano.
Saludos a la cámara!
Abrazos para ti!
he ido leyendo a trozos, no me he enterado de la mitad, pero ¡¡ te lo has currado ¡¡, mola la entrada
Muchas gracias!
Un post sencillamente genial que explica todo lo que hay que saber sobre el azúcar invertido y su utilización. Yo, como voy casi siempre con prisas, cuando hago helado y si el sabor me lo permite, cambio el 10% del total del azúcar que lleva la receta por miel y arreando!! Helado sin remover cada media hora, sin cristalización y ultra cremoso!! Te recomiendo hacer helado de plátano con este método, te encantará!
Lo de la miel es buena opción. Tomo nota! Tienes esa receta de helado de plátano en el blog? Saludos, Pablo.
Sí que la tengo!! Pero no puedo ponerte el enlace con el móvil, si entras en mi blog es el cuarto post que te encuentras, publiqué 3 entradas después ;D
Ya te contaré qué tal sale! Gracias.
Grandísimo Pablo! Lo primero de todo es que me he sentido totalmente identificada con la introducción, también por eso estudié ciencias, (aún reconociendo que naturalmente soy de letras), por satisfacer esa continua necesidad de saber de dónde vienen las cosas… y he de decir que el término azúcar invertido no me deja nada indiferente… me pide a gritos entender de dónde sale! o al menos eso, acercarse a comprender el porqué del término…, para seguir: no he podido evitar recordar mis clases de química de bachillerato, que en las de la carrera a lo de dextrógiro y levógiro molecularmente hablando, en Icai al menos, no se llegaba… y para terminar: no seré crítica con tu lección de química, entre otras cosas porque me falta entrenamiento para pararme a entender bien todo lo que explicas… sólamente tengo una pregunta ¿dónde compras el cremor tártaro? he leído esa palabreja mil veces en los libros de mi madre con los que empecé a cocinar y nunca supe donde encontrarlo! Un besote y enhorabuena por el articulo!
Jejejeje, no es para tanto; de hecho sigo picado porque hay un par de cosas que siguen sin cuadrarme… Lo del crémor tártaro, que suena muy sofisticado pero es ácido tartárico. De las míticas gaseosas o papeletes de dos colores encontrarás de dos tipos ácido cítrico-bicarbonato potásico y ácido tartárico(crémor)-bicarbonato potásico. Se utiliza en repostería para estabilizar merengues y alguna que otra cosa. Ahora a desempolvar esas recetas y ponerlas en práctica. Saludos.
Yo me he perdido casi todo. No estudio química desde 2º de bachillerato, que no se me daba mal, pero que me queda más o menos en la prehistoria. Sï que me interesa cómo funcionan las cosas, pero me temo que necesito una explicación para niños de básica :-(( Un currazo tu post, eso está claro.
Muchas gracias… Con quedarte que lo puedes hacer fácil en casa y las cantidades… 😉 Saludos!
Alucinado quedado me he! pedazo de post… éste es de los de subir nota. No suelo elaborar helados en casa y no sabía lo que era el azúcar invertido. Ahora podría decir que me queda más o menos claro y encima que me suena algo cómo poder aplicarlo. Muchas gracias!
Un saludo,
Gracias a ti! Me quedó un poco friki, pero disfruté con el repaso. Saludos!
Me llevo dando cuenta desde hace mucho tiempo que para saber los entresijos del porqué de las cosas en la cocina hay que leer y experimentar mucho. ¿Friki? podemos llamarlo así, pero ¿y lo que aprendemos?
Un saludo!
K si m lo explica un quimico lo entiendo igual, me salte alguna resolución k no llego a comprender… a mi tambien m gusta saber la raiz de las cosas pero en este caso ya no entro a descifrar todas esas cadenas….uf¡¡¡
Si hay tantas cosas así de complejas en reposteria mejor que con ésto se me quite la inquietud. Lo mio va por el merengue para decorar tartas que tambien lleba glucosa y claro tengo un ¨lio¨ con si es similar a el azucar invertido? entiendo con tu post que la sustituye en parte… t agradeceria que m lo confirmaras y bueno si sabes las proorciones para el merengue suizo que es el que quiero hacer. Gracias por ser tan curiosooooo¡¡¡¡¡
Hola Pablo!! (He visto tu nombre en comentarios anteriores). Nos ha encantado tu entrada, estábamos bicheando algunas dudas sobre el azúcar invertido y creo que nos has ayudado bastante. Comentarte que tenemos un página en facebook y twitter llamada «Química más Fácil» y observando tus niveles de frikismo químico, nos gustaría invitarte a conocer y participar en ella. Un Saludo!! Eres un crack! 😉
¿Pero por qué la sacarosa y el azúcar invertido tienen propiedades distintas si parten de la misma base?
Hola Sara,
Lo que sucede es que al «invertir» el azúcar conviertes la sacarosa en fructosa y glucosa y éstas tienen propiedades distintas de la sacarosas.
Saludos,
Pablo.
Buen dia, quiero elaborar helado apto para diabetico y no se que anticongelante conviene, se puede solo miel, como hago? gracias LAURA
Hurra por este post. Aunque el 90% de la gente no entienda ni papa.
Muy interesante, aun cuando no entiendo el despeje de las reacciones, me sirve de mucho tu anaslisis, me aclara dudas que tenia del procedimiento, gracias por el post
Hola, muy bueno tu articulo y la investigacion.
Soy pastelero y te puedo decir que en heladeria se limita el uso del azucar invertido, porque altera el punto de fusion/congelacion del helado.
Cada edulcorante tiene sus propiedades quimicas, pero tambiem tiene unas propiedades fisicas que actuan en la elaboracion.
El límite del 30 % tiene que ver con el poder endulzante del azúcar invertido, el cuál es un 30% mayor que el de la sacarosa.
Jisto ahora estoy estudiando eso y la D y la L no se refiere a si es dextrógiro o levógiro sino a la colocación del -OH de penúltimo carbono. Si este se encuentra a la derecha es D y si se encuentra a la izquierda es L.